Nota de seguridad de dispositivos médicos
Philips Respironics
Nota de seguridad 2021-05-A & Nota de seguridad 2021-06-A
Si aún no ha registrado el dispositivo
Noticias y actualizaciones > Información de seguridad del dispositivo de reemplazo
Comprenda los pasos que tomamos para garantizar la seguridad de su dispositivo CPAP o BiPAP de reemplazo
14 de diciembre de 2022
Mientras trabajamos para proporcionar dispositivos de reemplazo lo más rápido posible, queremos compartir los pasos que estamos tomando para garantizar que su dispositivo de reemplazo DreamStation de primera generación sea seguro de usar para que pueda confiar en su nuevo dispositivo.

Si bien los dispositivos afectados contenían un componente de espuma de reducción de sonido a base de poliuretano (PE-PUR), la espuma de reducción de sonido en todos los dispositivos nuevos y reformados es una espuma de silicona que ha cumplido con todos los estándares de prueba de la industria aplicables, incluidas las pruebas de emisiones de partículas y compuestos orgánicos volátiles (COV), y está autorizada como parte de nuestra remediación.
Todos los dispositivos nuevos y reformados incluirán una etiqueta en la parte inferior que indique REV15 o mayor. Este indica que el dispositivo ha sido remediado para incluir espuma de silicona y es seguro de usar.
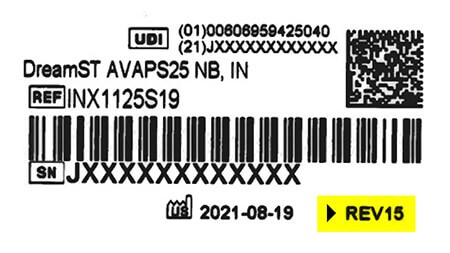

La limpieza y el mantenimiento regulares del dispositivo son importantes para su terapia

¿Necesita más información?
Por favor visite www.philips.com/SRC-Update

